목차
- 소포체란 무엇인가? 세포 안의 데이터 센터
- 소포체 스트레스: 시스템 과부하와 예외 처리
- 단백질 품질 관리 시스템의 붕괴와 노화
- 소포체 기능 이상이 유발하는 주요 질병
- 최신 바이오테크놀로지를 통한 기능 회복 연구
- 결론 및 참고 자료
생명체를 구성하는 가장 기본 단위인 세포 내부에는 거대하고 정교한 산업 단지가 조성되어 있습니다. 이 중에서 단백질의 생산, 가공, 검수, 그리고 배송을 총괄하는 핵심 인프라가 바로 ‘소포체(Endoplasmic Reticulum, ER)’입니다. 현대 생물학과 의학은 단순히 소포체를 세포 소기관 중 하나로 보는 것을 넘어, 인체의 노화 속도를 결정짓고 다양한 난치성 질병을 유발하는 마스터키로 인식하고 있습니다. 정상적인 단백질 생산 라인에 문제가 발생하여 불량 단백질이 축적될 때, 우리 몸의 시스템은 심각한 타격을 입게 됩니다. IT 관점에서 보면 이는 잘못 컴파일된 코드가 시스템 메모리를 점유하여 결국 서버를 다운시키는 과정과 매우 흡사합니다. 본 포스팅에서는 소포체의 기본 원리부터 소포체 스트레스(ER Stress)가 노화와 질병에 미치는 영향, 그리고 이를 극복하기 위한 최신 연구 동향까지 상세히 분석해 보겠습니다.
소포체란 무엇인가? 세포 안의 데이터 센터
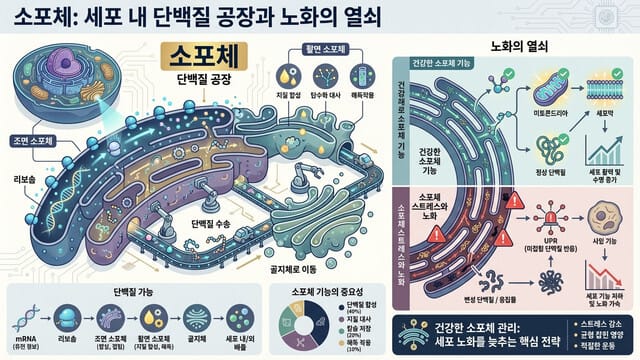
소포체(Endoplasmic Reticulum)는 진핵세포 내부에 존재하는 막으로 둘러싸인 복잡한 네트워크 구조물입니다. 소포체는 크게 표면에 리보솜(Ribosome)이 붙어 있는 ‘조면소포체(Rough ER)’와 리보솜이 없는 ‘활면소포체(Smooth ER)’로 나뉩니다.
이를 IT 시스템에 비유하자면, 조면소포체는 프로그래머가 작성한 소스 코드(mRNA)를 넘겨받아 실제 실행 가능한 소프트웨어 프로그램(단백질)으로 ‘컴파일(Compile)’하는 거대한 서버 팜과 같습니다. 리보솜에서 합성된 아미노산 사슬은 조면소포체 내부로 들어가 3차원 구조로 정교하게 접히는 폴딩(Folding) 과정을 거치게 됩니다. 단백질은 이 3차원 구조를 완벽하게 갖추어야만 본연의 기능을 수행할 수 있습니다.
반면, 활면소포체는 지질 합성, 스테로이드 호르몬 생성, 해독 작용, 그리고 칼슘 이온(Ca2+)의 저장고 역할을 담당합니다. 이는 시스템의 보안(해독)과 데이터베이스 스토리지(칼슘 저장) 역할을 수행하는 백엔드 인프라에 비유할 수 있습니다. 세포가 외부 자극을 받아 신호를 전달해야 할 때, 활면소포체는 저장해 둔 칼슘을 세포질로 방출하여 즉각적인 반응을 이끌어냅니다. 이처럼 소포체는 단순한 공장이 아니라, 세포라는 거대한 운영체제(OS)가 원활하게 돌아가도록 돕는 핵심 데이터 센터이자 프로비저닝 인프라입니다.
소포체 스트레스: 시스템 과부하와 예외 처리
컴퓨터 시스템에 트래픽이 폭주하거나 버그가 발생하면 서버에 과부하가 걸리듯, 세포 내 환경 변화나 유전적 요인으로 인해 소포체 내부에 제대로 접히지 않은 ‘미접힘 단백질(Unfolded Protein)’이나 엉뚱하게 접힌 ‘오접힘 단백질(Misfolded Protein)’이 쌓이게 되면 소포체는 심각한 과부하 상태에 빠집니다. 생물학에서는 이를 소포체 스트레스(ER Stress)라고 부릅니다. 잘못된 단백질은 시스템의 메모리 누수(Memory Leak)를 일으키는 악성 코드와 같습니다.
이러한 위기 상황을 극복하기 위해 소포체는 자체적인 예외 처리(Exception Handling) 메커니즘을 가동하는데, 이를 미접힘 단백질 반응(UPR, Unfolded Protein Response)이라고 합니다. UPR은 주로 IRE1, PERK, ATF6라는 세 가지 센서 단백질을 통해 작동합니다.
- 단백질 합성 중단 (Traffic Control): PERK 경로는 새로운 단백질의 유입을 일시적으로 차단하여 소포체의 작업 부담을 줄입니다. 서버에 들어오는 신규 요청(Request)을 차단하는 로드 밸런싱의 일환입니다.
- 샤페론 단백질 증량 (Scaling Up): ATF6와 IRE1 경로는 단백질 폴딩을 돕는 ‘샤페론(Chaperone)’이라는 도우미 단백질의 생산을 급격히 늘립니다. 이는 트래픽 처리를 위해 클라우드 서버의 인스턴스를 오토 스케일링(Auto-scaling)하는 것과 같습니다.
- 불량 단백질 폐기 (Garbage Collection): 도저히 복구할 수 없는 불량 단백질은 세포질로 배출되어 프로테아좀(Proteasome)에 의해 분해됩니다. 완벽한 가비지 컬렉션(GC) 프로세스입니다.
하지만 이러한 UPR 메커니즘으로도 해결할 수 없을 만큼 심각한 스트레스가 지속되면, 소포체는 스스로 세포 사멸(Apoptosis)을 유도합니다. 즉, 전체 시스템(조직)을 보호하기 위해 감염되거나 고장 난 노드(세포)의 전원을 강제로 차단해 버리는 OOM Killer(Out of Memory Killer) 로직이 발동하는 것입니다.
단백질 품질 관리 시스템의 붕괴와 노화
인간의 몸이 나이가 들면 IT 인프라가 노후화되듯, 세포 내부의 단백질 품질 관리(Protein Quality Control, PQC) 시스템도 그 효율성을 서서히 잃게 됩니다. 앞서 언급한 샤페론 단백질의 활동성이 떨어지고, UPR의 예외 처리 능력이 둔화되는 것이 바로 세포 노화(Cellular Senescence)의 핵심 원인 중 하나입니다.
젊고 건강한 세포에서는 불량 단백질이 발생하더라도 즉각적인 디버깅(Debugging)과 가비지 컬렉션이 이루어집니다. 하지만 노화가 진행된 세포에서는 소포체가 스트레스에 적절히 대응하지 못하여 불량 단백질이 세포 내부에 거대한 찌꺼기(Aggresome) 형태로 축적됩니다. 이러한 비정상적인 단백질 덩어리들은 세포 내 다른 정상적인 오르가넬라(세포 소기관)들의 물리적, 화학적 작용을 방해하며 만성적인 염증 수치를 높입니다.
결과적으로 소포체의 기능 저하는 단순히 세포 하나의 늙어감을 의미하는 것이 아니라, 전신에 걸친 대사 저하와 면역력 감소, 그리고 조직 재생 능력의 상실로 이어집니다. 최근 항노화(Anti-aging) 연구 분야에서는 이 소포체의 품질 관리 기능을 젊은 시절의 수준으로 리셋(Reset)하거나 활성화하는 물질을 찾는 데 막대한 자본과 IT 기술력을 투자하고 있습니다.
소포체 기능 이상이 유발하는 주요 질병
소포체 스트레스와 단백질 접힘 이상은 현대 의학이 직면한 여러 난치성 질환의 직접적인 원인으로 지목되고 있습니다.
첫째, 퇴행성 뇌질환입니다. 알츠하이머병, 파킨슨병, 헌팅턴병 등은 모두 특정 불량 단백질이 뇌세포 내에 축적되어 발생합니다. 알츠하이머병의 아밀로이드 베타(Amyloid Beta)나 파킨슨병의 알파-시뉴클레인(Alpha-synuclein) 단백질은 소포체의 가비지 컬렉션 기능이 고장 났을 때 분해되지 못하고 신경세포를 파괴합니다. 뇌세포는 한 번 파괴되면 복구가 매우 어렵기 때문에, 소포체 기능 저하는 치명적인 결과를 초래합니다.
둘째, 대사성 질환입니다. 제2형 당뇨병이 대표적입니다. 췌장의 베타세포는 혈당을 조절하기 위해 쉴 새 없이 인슐린 단백질을 생산해야 하는 엄청난 업무 강도에 시달립니다. 비만이나 과도한 영양 섭취가 지속되면, 소포체는 쏟아지는 인슐린 생산 요청을 감당하지 못하고 극심한 소포체 스트레스에 빠집니다. 결국 앞서 설명한 세포 사멸(Apoptosis) 스위치가 켜지면서 췌장 베타세포가 파괴되고, 이는 인슐린 분비 장애와 중증 당뇨병으로 직결됩니다.
셋째, 다양한 암(Cancer)과도 연관이 깊습니다. 역설적으로 암세포는 영양이 부족하고 산소가 모자란 극한의 환경에서도 빠르게 증식해야 하므로 극도의 소포체 스트레스를 경험합니다. 하지만 암세포는 UPR 메커니즘을 교묘하게 해킹하여 스스로를 보호하는 생존 전략으로 악용합니다. 따라서 암세포의 UPR 스위치를 강제로 끄거나 과도하게 자극하여 사멸을 유도하는 항암제 개발이 활발히 이루어지고 있습니다.
최신 바이오테크놀로지를 통한 기능 회복 연구
최근 IT와 바이오테크놀로지의 융합을 통해 소포체의 기능을 회복하고 질병을 근본적으로 치료하려는 혁신적인 연구들이 진행되고 있습니다. 단백질의 3차원 접힘 구조를 완벽하게 예측하는 딥마인드의 ‘알파폴드(AlphaFold)’와 같은 AI 기술은, 소포체 내에서 특정 단백질이 왜 잘못 접히는지 그 알고리즘을 해독하는 데 결정적인 기여를 하고 있습니다.
의학계에서는 화학적 샤페론(Chemical Chaperone)이라는 약물을 통해 소포체의 부담을 덜어주는 치료제를 개발 중입니다. 대표적으로 TUDCA(Tauroursodeoxycholic acid)나 PBA(Sodium phenylbutyrate)와 같은 물질들이 소포체 스트레스를 완화하여 퇴행성 뇌질환이나 당뇨병 치료에 임상적 가능성을 보여주고 있습니다. 또한, 특정 UPR 센서(예: PERK 억제제)를 표적으로 하는 저분자 화합물들이 새로운 항암제로 각광받고 있습니다.
이러한 바이오 데이터와 단백질 구조 분석 기술은 향후 IT 전문가들에게도 폭넓은 기회를 제공할 것입니다. 생물학적 메커니즘을 데이터 베이스화하고 알고리즘으로 분석하는 능력이 필수적으로 요구되기 때문입니다. 만약 관련 분야의 전문 지식을 입증하고 바이오 산업으로의 진출을 모색하고자 한다면, 다가오는 2024년 11월 20일에 실시되는 ‘바이오메디컬 데이터 분석 전문가(BMDA) 국가공인 자격증 심화 과정 및 평가 시험’과 같은 전문 교육 일정에 참여하여 바이오인포매틱스 역량을 기르는 것을 적극 권장합니다.
결론 및 참고 자료
지금까지 세포 내 단백질 공장인 소포체의 역할과 소포체 스트레스가 인체의 노화 및 질병에 미치는 방대한 메커니즘을 살펴보았습니다. 소포체는 단순히 생물학적 부품이 아니라, 인체라는 거대한 네트워크 시스템의 무결성을 유지하는 핵심 데이터 센터입니다. 잘못된 식습관, 과도한 스트레스, 노화로 인해 발생하는 단백질 품질 관리 시스템의 붕괴는 알츠하이머, 당뇨, 암 등 치명적인 시스템 오류를 발생시킵니다.
앞으로 AI와 바이오인포매틱스 기술의 발전은 소포체의 비밀을 완전히 해독하고, 인류가 노화와 질병의 굴레에서 벗어나는 데 중추적인 역할을 할 것입니다. IT와 생명과학이 만나는 이 거대한 패러다임의 변화에 지속적인 관심을 가져보시길 바랍니다.